分享到:
- 微信
- 微博
恒瑞医药12月21日晚发布公告称,近日公司就抗PD-1抗体SHR-1210联合甲磺酸阿帕替尼一线治疗肝细胞癌的国际多中心III期临床试验与美国食药监局(FDA)进行了沟通,该试验即将在美国、欧洲和中国同步开展。FDA同意即将开展的Ⅲ期临床试验并在无进展生存期期中分析结果达到预设的统计学标准时提前申报生产,这意味着此次申请如最终通过,将获加速审评。
公告称,SHR-1210是恒瑞医药自主研发的,具有完全自主知识产权的人源化抗PD-1抗体,可用于血液恶性肿瘤和实体瘤的治疗。甲磺酸阿帕替尼是恒瑞医药创新研发的针对晚期胃癌的的小分子靶向药物,2014年在国内获批上市。
公告还提示,按照美国药品注册相关法律法规的规定,美国FDA自受理之日起30日内未下发“暂停临床试验”或“暂停部分临床试验”通知的,可获准进行临床试验。由于临床试验检验、审评和审批周期长、环节多,容易受到一些不确定性因素的影响,后续开展的Ⅲ期临床试验的无进展生存期期中分析结果如果未达到预设的统计学标准将无法提前申报生产。
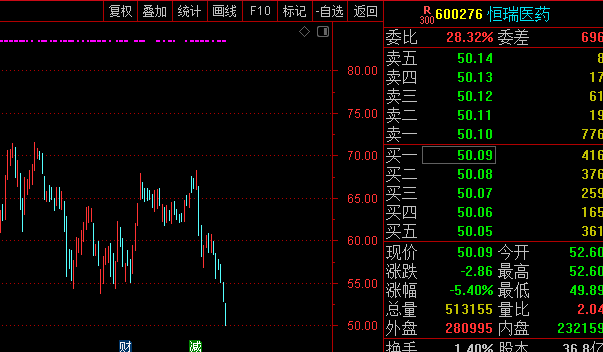
12月21日收盘,恒瑞医药重挫5.4%报收50.09元,股价创出年内新低。受“带量采购”新政影响,恒瑞医药本周下跌14.96%,月内跌幅更是高达23.47%。

恒瑞医药计划近期递交双靶点减肥药上市申请
恒瑞医药计划近期在中国递交HRS9531注射液用于长期体重管理的新药上市申请。

多款创新器械和药物亮相东方会,心血管疗法有望打破“姑息治疗”
在心血管领域的治疗方面,过去临床上很多疗法都是姑息治疗,例如心衰或者严重的瓣膜疾病,很多时候患者来就医时,疾病已经发展到终末期了,没有很好的治疗方法。

折价发行,恒瑞医药港股股价首日开盘涨三成
本次港股IPO,恒瑞医药确定的发行价最终为44.05港元/股,较A股5月22日55.40元/股的收盘价折价近27%(按照当天港元对人民币中间价计算)左右。

A股龙头掀H股上市潮,港股行情将如何延续?|市场观察
对比2019年到2021年中概互联网公司回归,本轮IPO热潮更多集中于新质生产力企业。

高瓴抛售百济神州套现21亿港元,要去认购恒瑞医药新股
趁着股价反弹,高瓴资本今年多次减持百济神州美股股份。