分享到:
- 微信
- 微博


{{aisd}}
AI生成 免责声明
创新药企盛诺基的科创板IPO审核已在问询环节停滞了近16个月,是目前该环节受理时间最长的一家公司。
对于盛诺基一直停滞不前的原因,第一财经记者多次联系该公司披露的电话,均未有人应答。
从交易所对盛诺基进行的四轮问询来看,关注的焦点主要在于:一是盛诺基核心产品阿可拉定的未来市场空间;二是在研产品SNG1005是盛诺基通过关联方香港欣诺康引自国外,此模式是否合理,三方是否存在纠纷以及权益如何划分;三是盛诺基达到盈亏平衡所需的条件和时间。
盛诺基拟采用科创板第五套标准亏损上市。截至10月17日,科创板共有10家公司选择了该标准挂牌上市,且均为生物医药行业公司。这些公司成功上市的关键点在于有核心技术且有接近商业化的在研药品。
阿可拉定是盛诺基最为接近新药上市及商业化的核心在研药品。而在竞品索拉非尼仿制药陆续上市,与阿可拉定适应症相同的多纳非尼已上市等背景下,阿可拉定面临的市场竞争风险加剧,前景不明。
IPO停滞不前
盛诺基的科创板IPO申请于2020年5月28日获受理,一个月后的6月28日进入问询阶段,但之后的一年多仍旧停滞于该环节,目前尚未有新的进展。
2020年8月4日,盛诺基回复了交易所的第一轮问询。2020年9月29日,盛诺基因发行上市申请文件中记载的财务资料已过有效期,需要补充提交,被中止审核,直至2020年12月31日公司IPO申请恢复审核。
之后,盛诺基相继回复了交易所的第二轮、第三轮、第四轮问询,并根据2020年报和2021年半年报更新相关信息。
四轮问询整体来看,聚焦的问题主要在发行人核心技术、发行人业务、市场空间、股份支付、研发费用、公司治理与独立性、财务会计信息与管理层分析、重大事项提示和风险因素等方面。
其中被追问最多的便是盛诺基两大产品——阿可拉定和SNG1005的相关问题,以及向盛诺基出租办公用房产的健赞生物是否占用盛诺基资金。具体来看,比如:视实际情况,有针对性、充分地揭示因靶点较为新颖或目前针对该靶点开发的药物较少所带来的作用机制不够明确,科学研究或经验不足,从而导致阿可拉定研发失败概率较高、上市进展不及预期的风险;又如:SNG1005进展情况如何,盛诺基需要充分揭示SNG1005未来研发失败或进度不及预期,面临的市场竞争风险。
阿可拉定和SNG1005是盛诺基比较核心的两个在研产品。盛诺基是一家以中药现代化和生物科技相结合,专注于肝细胞癌、乳腺癌、非小细胞肺癌、淋巴瘤等多个恶性肿瘤领域,以中药创新药为先导,并延伸布局化学创新药和生物大分子创新药的医药研发企业。
据预披露招股说明书(下称“招股书”),该公司拥有13个在研产品的21项在研项目,其中,在研药品阿可拉定正在进行两项III期临床试验;在研药品SNG1005的两个适应症已经分别获得II/III期和III期临床试验通知书;在研药品氟可拉定已获I期临床试验批准,同时亦获美国临床试验批准。其余9个在研药品均处于临床前研究阶段;此外,公司ER-α36(新型雌激素受体)临床诊断试剂盒已完成临床试验。
但是,根据9月30日披露的2021年半年报更新版的问询回复,该公司所有产品处于研发阶段,尚未有药品上市,无经常性营业收入产生。公司未来产生收入主要取决于公司主要产品的研发成功和商业化目标顺利实现。
因无销售收入,2017年度~2019年度,该公司归母净利润分别亏损8458.14万元、1.28亿元和3.12亿元;同期,该公司研发费用分别为4581.68万元、7649.89万元及1.28亿元。
盛诺基拟采用第五套上市标准在科创板上市募资20.24亿元,用于肿瘤和糖尿病新药研发项目、化学合成原料药SNG-1153和 SNG-1005生产建设项目以及营运及发展储备资金。
就目前的审核情况来看,盛诺基能否成功上市还待观察。
核心在研产品阿可拉定是关键
作为盛诺基的核心在研产品,阿可拉定的上市进展以及商业化前景对公司至关重要,影响其未来的业务发展及业绩,也是市场关注的焦点。
盛诺基在2020年5月28日披露的招股书中介绍,阿可拉定是源于传统中药材淫羊藿采取现代生物技术研制的小分子免疫调节创新药(First-in-class),在治疗晚期肝细胞癌且对不适于现有化疗药物及靶向药物治疗的患者具有显著安全性和确切疗效,已进入III期临床试验,计划于2021年3月份提交NDA申请(新药上市申请)。
2021年3月12日,阿可拉定的Pre-NDA沟通交流会召开。2021年4月10日,CDE正式受理阿可拉定NDA申请。2021年5月18日,阿可拉定被正式纳入优先审评审批程序。
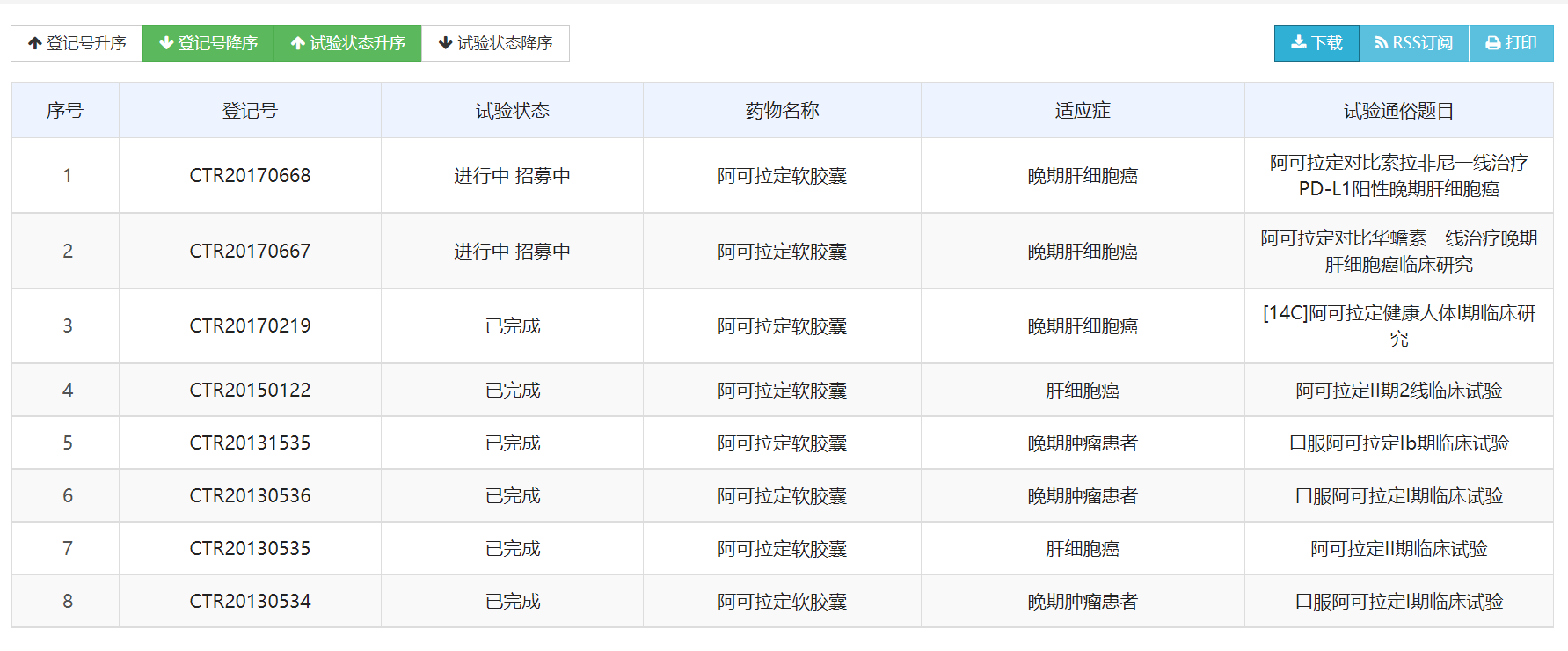
第一财经记者查阅药物临床试验登记与信息公示平台发现,阿可拉定对比索拉非尼一线治疗PD-L1阳性晚期肝细胞癌、对比华蟾素一线治疗晚期肝细胞癌临床研究这两项实验目前仍在进行、招募中。
值得注意的是,阿可拉定的竞品之一索拉非尼化合物专利已到期,仿制药上市将加剧市场竞争的风险。据国家知识产权局网站信息,索拉非尼在中国的化合物专利已于2020年1月到期,晶型专利将于2025年9月到期。市场上索拉非尼仿制药将陆续上市,而仿制药的价格通常显著低于原研药。若仿制药被纳入医保目录,病人支付价格会进一步降低。
盛诺基也称,索拉非尼仿制药的上市, 将加剧肝细胞癌用药市场竞争,进而可能会对该公司的经营业绩和发展前景产生不利影响。
另外,今年6月份,泽璟制药(688266.SH)的1类创新药甲苯磺酸多纳非尼片(下称“多纳非尼片”) 获批上市,用于既往未接受过全身系统性治疗的不可切除肝细胞癌患者。10月17日晚间,泽璟制药公告称,多纳非尼片用于治疗局部晚期/转移性放射性碘难治性分化型甲状腺癌(RAIR-DTC)的新适应症上市申请获得受理。
交易所也曾在问询中提及,阿可拉定的临床试验进度、预计上市时间是否落后于仿制药多纳非尼或其他同类药品,该等情形对阿可拉定未来市场空间的影响,是否会制约阿可拉定未来的市场空间。
对此,盛诺基回复称,索拉非尼仿制药及多纳非尼的上市主要会在使用索拉非尼原研药的患者群体间竞争,不适用索拉非尼的患者群体需求依然缺乏合适的药物。阿可拉定在此方面具有优势,可填补该类患者的用药空白。
但是,盛诺基也提示风险称,该公司最为接近新药上市及商业化的核心在研药品阿可拉定可能存在无法按照预期时间提交新药上市申请的情形,或者即使按照预期提交新药上市申请,能否于预期时间内顺利获得监管机构批准上市亦存在不确定性。如核心在研药品阿可拉定的新药上市进程受到较大程度的延迟,则将对公司未来的业务及经营业绩造成较大不利影响。
“除阿可拉定外的其他核心临床在研产品中,盛诺基授权引进药物SNG1005的研发计划受境外药品供应影响而延迟,III期临床试验预计推迟至2021年11月开始;ER-α36诊断试剂盒预计于2021年进行NDA申请;原计划2020年于美国启动的氟可拉定I期临床试验受新冠疫情影响,计划推迟至2021年开始。”盛诺基在第四轮问询回复中称。
如需获得授权请联系第一财经版权部:banquan@yicai.com