分享到:
- 微信
- 微博


{{aisd}}
AI生成 免责声明
吉利德科学旗下药物拓达维®,在中国获批用于转移性三阴性乳腺癌的二线治疗,预计在今年第四季度商业化上市。
6月10日,云顶新耀(1952.HK)宣布了这一结果。国家药品监督管理局于2021年5月接受了其上市许可申请,批准拓达维®(Trodelvy®,戈沙妥珠单抗)用于既往至少接受过2种系统治疗(其中至少一种治疗针对转移性疾病)的不可切除的局部晚期或转移性三阴性乳腺癌成人患者。
根据与吉利德科学公司签署的授权协议,云顶新耀在大中华区、韩国和部分东南亚国家享有针对拓达维®所有癌症适应症开发、注册和商业化的独家权利。拓达维®也是云顶新耀获准在中国上市的首款创新药品。
2021年11月,云顶新耀公布了戈沙妥珠单抗2b期EVER-132-001研究的顶线结果,该研究以38.8%的客观缓解率达到其主要终点。这项研究在中国的80名患者中开展,所得结果与全球3期ASCENT研究的结果一致,因此显示其在中国人群中具有相似的疗效和安全性。
三阴性乳腺癌是一种高度侵袭性疾病,约占全球所有乳腺癌类型的15%。在亚洲,乳腺癌的确诊年龄中位数与西方国家相比有年轻化趋势,近10年来,三阴性乳腺癌分子亚型的比例逐年上升。
与其他类型的乳腺癌相比,三阴性乳腺癌的有效治疗方案极其有限。且三阴性乳腺癌比其他类型的乳腺癌复发和转移的几率更高。三阴性乳腺癌转移复发的平均时间约为2.6年,而其他乳腺癌为5年,相对的5年生存率更低。在转移性三阴性乳腺癌女性患者中,5年生存率为12%,而其他类型转移性乳腺癌患者的5年生存率为28%。
中国工程院院士、国家新药(抗肿瘤)临床研究中心主任、拓达维中国注册研究主要研究者徐兵河表示,三阴性乳腺癌患者临床上急需新的有效治疗方案。
拓达维®是一款同类首创的抗体偶联药物,靶点为Trop-2受体。目前,拓达维®已在超过35个国家/地区获批用于治疗既往接受过至少两种系统治疗(其中至少一种为针对转移性疾病的治疗)的不可切除的局部晚期或转移性三阴性乳腺癌成人患者。
2020年10月,拓达维®被纳入到2020版《中国晚期乳腺癌规范诊疗指南》。2021年10月,被纳入《中国抗癌协会乳腺癌诊治指南与规范(2021)》。2022年4月又被纳入《2022中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》。同月,首次被纳入中国台湾地区的《台湾乳房医学会三阴性乳癌治疗共识手册(2022年版)》。
除了中国大陆以外,今年1月,新加坡卫生科学局也批准了拓达维®的新药上市申请,用于转移性三阴性乳腺癌二线及后期治疗。目前,包括韩国、中国台湾地区和香港地区也已经受理了其新药上市申请。
如需获得授权请联系第一财经版权部:banquan@yicai.com
文章作者

我国儿童肿瘤生存率首次纳入年报体系!5年达76.42%,不同癌种差异显著
5年生存率最高的前五位依次为:视网膜母细胞瘤、恶性上皮肿瘤和黑色素瘤、生殖细胞肿瘤、淋巴瘤和肾肿瘤。

乳腺癌、胰腺癌盯上年轻人,男性过早死亡率出现双增长
考虑到人口老龄化和普遍存在的不健康生活方式,全球及中国的癌症相关死亡人数预计继续上升
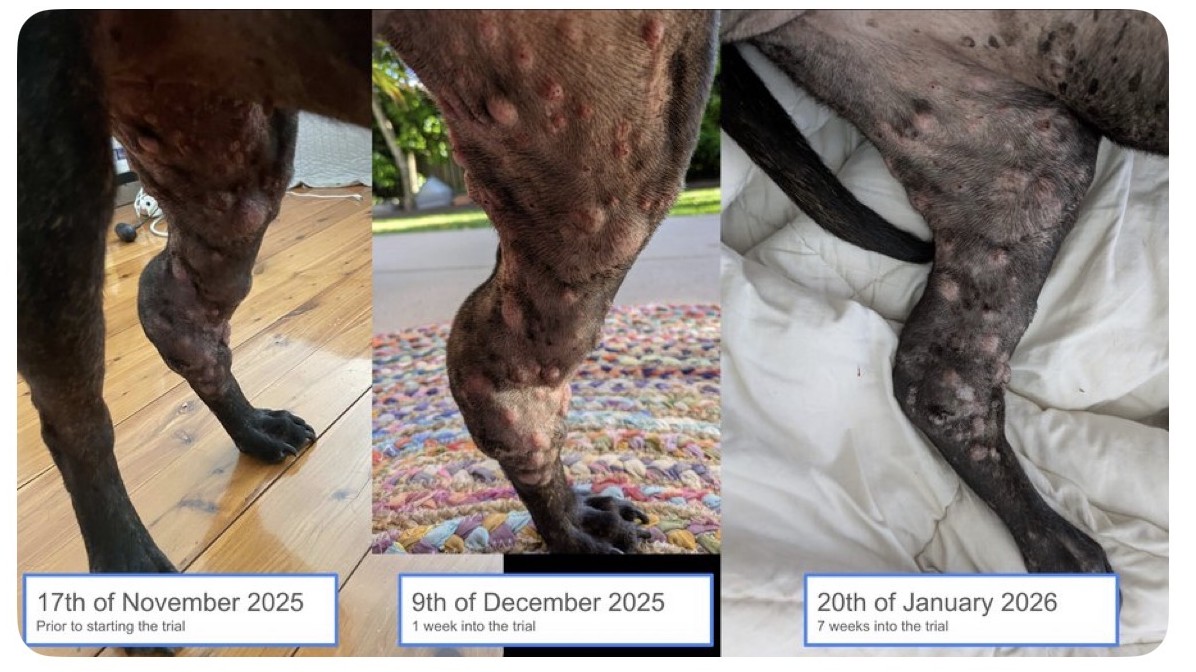
程序员用AI手搓疫苗抢救患癌爱犬,马斯克等大佬点赞
动物实验转化为人类临床仍有漫长道路。

中国癌症五年生存率稳步提升,多学科协作成破局关键
尽管肿瘤诊疗已迈入精准医疗时代,但临床实践中仍面临诸多待解难题
“布拉格峰”改写抗癌逻辑,质子技术重塑肿瘤治疗新路径
被誉为 “精准抗癌利器” 的质子治疗。
