分享到:
- 微信
- 微博


{{aisd}}
AI生成 免责声明
随着全球秋季疫苗接种季到来,辉瑞/BioNTech和Moderna已竞相向美国FDA递交授权申请,寻求奥密克戎新版疫苗的批准。
周二,Moderna向美国FDA递交了针对奥密克戎BA.4/BA.5变异株以及新冠原始毒株的二价加强疫苗申请,该疫苗区别于该公司已经在英国获得批准的一款二价疫苗,英国批准的疫苗针对BA.1变异株和新冠原始毒株。

美国药监机构一直在要求制药厂商针对最新流行的奥密克戎BA.4/BA.5变异株开发疫苗。Moderna并表示如果获得批准,它将准备在9月交付疫苗。该公司还称,该疫苗的中后期试验正在进行中。
就在Moderna宣布这一消息的前一天,竞争对手辉瑞及其德国合作伙伴BioNTech也向美国FDA递交申请,寻求针对奥密克戎BA.4/BA.5以及新冠原始毒株的二价疫苗加强剂的授权。辉瑞表示,这些疫苗将在获得监管许可后立即发货。
辉瑞的疫苗申请是供12岁及以上人群紧急使用,而Moderna寻求的疫苗授权是供18岁及以上人群中使用。
不过由于美国FDA并不强制要求企业递交针对BA.4/BA.5的临床试验数据,有专家质疑这些新版疫苗与原始疫苗相比较的有效性是否显著增强。
美国得克萨斯州贝勒医学院的传染病和疫苗专家彼得·霍特茨教授(Peter Hotez)博士对第一财经记者表示,如果FDA仅仅基于小鼠数据就批准该疫苗,会令他感到惊讶。“我们值得等待更长的时间,来获取针对奥密克戎变异株疫苗的人体数据,这可能需要再花几周时间。”霍特茨说道。
自2021年新冠疫苗在全球大范围接种以来,mRNA疫苗在疫苗的分发竞赛中遥遥领先于竞争对手。这受益于mRNA平台的快速响应速度,一旦有新冠变异株出现,该平台也能灵活快速地调整配方,以研发出适应新的变异株的疫苗。
截至今年第二季度,BioNTech已向全球供应了36亿剂疫苗,尽管疫苗需求有所下降,但该公司第二季度收入仍然达到32亿欧元。
相比之下,与mRNA疫苗几乎同一批获准上市的腺病毒载体疫苗以及刚刚上市不久的重组蛋白疫苗在上市后的使用和市场占有方面遭遇了更大的阻碍,一些厂商不得不“认输”。
阿斯利康CEO帕斯卡尔·索里奥特(Pascal Soriot)周二在接受媒体采访时表示,从长远来看,该公司可能不会继续从事疫苗业务。阿斯利康在新冠疫情暴发后,与牛津大学合作,成为首批为全球提供新冠疫苗的厂商之一,但此后输给了竞争对手。
阿斯利康的疫苗获批后,曾经历生产延迟,并由于疫苗产生的罕见严重副作用而遭遇调查,这些坎坷都阻碍了该疫苗的采用。尽管阿斯利康在全球交付了数十亿剂新冠疫苗,去年收入达到39亿美元,但直到目前,该公司的新冠疫苗仍未获得美国批准。
重组蛋白疫苗厂商Novavax公司在8月8日公布的财报中,将其2022年的销售下调了约50%,调整后的全年收入在20亿至23亿美元。
但阿斯利康和Novavax的经验并未阻碍“后来者”进军新冠疫苗的决心,目前包括葛兰素史克(GSK)和赛诺菲在内的欧洲制药厂商,希望在加强疫苗市场中挑战美国mRNA疫苗的主导地位。
GSK新上任的疫苗研发负责人菲尔·多米策(Philip Dormitzer)近日表示:“初步数据显示,与mRNA疫苗相比,这种重组蛋白疫苗的副作用更少且抗体持续时间更长。”
GSK和赛诺菲在研的一款新冠二价重组蛋白疫苗已经处于临床试验后期,在错过第一波新冠疫苗市场后,两家公司期待于今年晚些时候提供这种疫苗。
如需获得授权请联系第一财经版权部:banquan@yicai.com
文章作者
制药巨头警告:欧洲可能沦为制药行业的“销售办事处”
根据研究公司Global Data的一项最新数据分析,自去年5月美国药品降价政策实施以来,欧洲新药在美国上市数量下降了约三分之一。

礼来CEO与清华校长面对面,跨国医疗企业在中国有哪些AI布局
学术界与产业界在创新链条中各具优势,要真正实现创新,需要把科研探索、临床验证与产业化落地连接成更顺畅的链路。

参与了26场“国谈”后,阿斯利康的“金牌谈判手”走了
黄彬是阿斯利康市场准入部的核心,曾带队参与多年国家医保谈判,累计参与26场谈判,推动德曲妥珠单抗、卡匹色替片等多款创新药纳入医保,对新药在中国的定价拥有丰富经验。
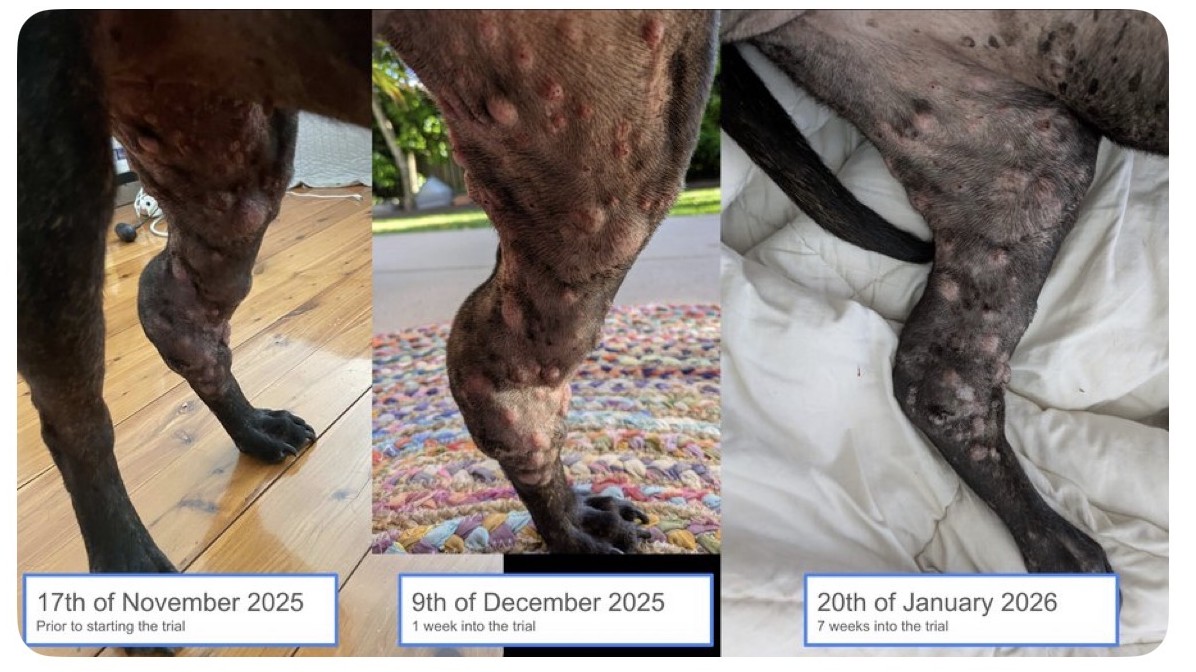
程序员用AI手搓疫苗抢救患癌爱犬,马斯克等大佬点赞
动物实验转化为人类临床仍有漫长道路。

雷海潮:我们应该有更多疫苗,更好更多的检验检测手段
加强公共卫生体系能力建设是国家卫健委未来五年将着力的重点方向。
