分享到:
- 微信
- 微博


{{aisd}}
AI生成 免责声明
9月29日,印度尼西亚国家食品药品监管局宣布,授予我国新型冠状病毒mRNA疫苗AWcorna紧急使用授权(EUA),用于18周岁及以上人群通过主动免疫来预防新冠病毒肺炎。
这是我国首款获得紧急使用授权批准的mRNA新冠疫苗,标志着我国在这一新型疫苗技术路线方面取得的重大进展。
AWcorna是由沃森生物和苏州艾博两家公司共同研发的一款针对新冠原始毒株的mRNA疫苗,不过三期大规模有效性临床试验数据尚未发表。据第一财经记者了解,EUA可以不用等到三期数据发表即可予以授权。
9月30日开盘后,沃森股价上涨超过3%,随后涨幅收窄。
据介绍,印尼最新批准的AWcorna在云南沃森疫苗工厂生产,可以在2-8摄氏度下储存,可以在常规冷链条件下储运,临用前无需解冻。未来这款疫苗也有望在印尼实现本地化生产。
该疫苗也是我国首个获批进入临床试验的新冠mRNA疫苗,据沃森方面介绍,目前公司还在积极推进该疫苗在中国的紧急使用授权申请。早在今年4月,沃森生物就曾对外宣称,国内新冠mRNA三期临床的现场工作基本结束,正在进行数据整理和持续血清检测。
沃森生物董事长李云春表示:“目前我国已经完全掌握了mRNA疫苗的关键核心技术,并且在主要原辅料与设备等全供应链上,完全实现了国产化自主可控。”
中国其他疫苗厂商也在加速mRNA技术路线的新冠疫苗的研发,除了沃森和艾博之外,已获得中国药监部门的临床批件的还有康希诺、斯微生物、石药集团等。其中,康希诺的mRNA疫苗在国内处于二期临床阶段,斯微生物的mRNA疫苗处于一期临床阶段。
沃森和艾博也在各自分头研发针对奥密克戎变异株的新版疫苗。艾博生物针对奥密克戎变异株的新冠病毒mRNA疫苗已经在阿联酋获临床批件;沃森生物则与上海蓝鹊生物合作开发新版疫苗,该疫苗已正式获得国家药品监督管理局临床试验批准,并开展临床一期试验。
尽管新技术路线疫苗的研发进展令人鼓舞,但专家表示,疫苗从研发到临床再到紧急授权批准需要一个相当漫长的过程。“在等待过程中,脆弱人群仍然应该尽早接种现有的疫苗和疫苗加强剂,而不要等待还在临床中的疫苗上市后才去接种,这样会导致更高的感染和重症风险。”一位公共卫生专家对第一财经记者表示。
如需获得授权请联系第一财经版权部:banquan@yicai.com
文章作者
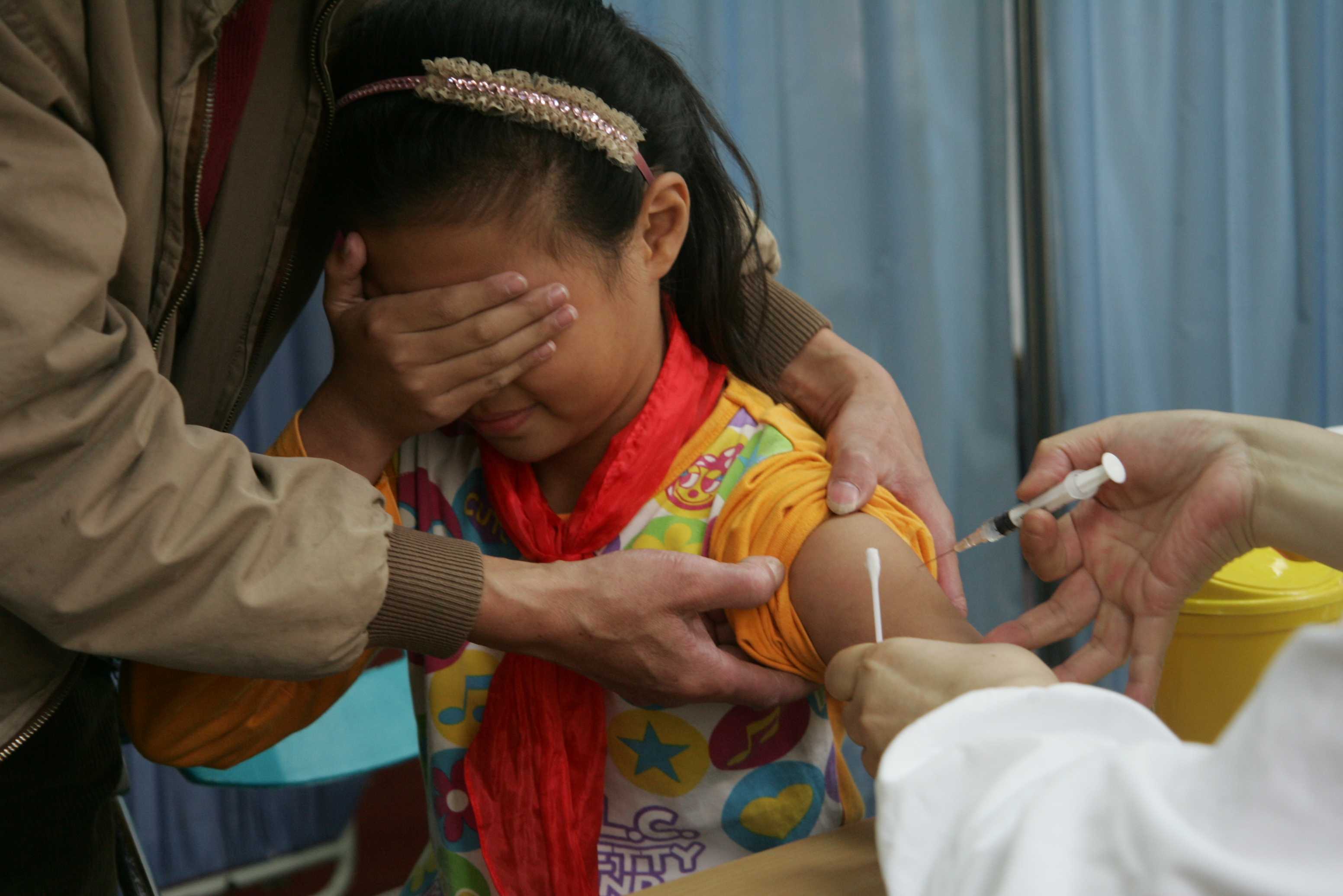
自费流感疫苗也可医保报销了
将流感疫苗进一步纳入国家免疫规划仍有必要
87人死亡!这一国第17次暴发埃博拉疫情,已上市的埃博拉疫苗为何不管用
全球已获批上市的埃博拉疫苗已有三款。

美国FDA一把手被罢免,医疗企业股价上涨
马卡里总结了自己任期内的一系列政策成果,包括缩短部分新药的审批周期,支持精神类药物的研发,以及扩大更年期激素疗法的使用范围。

疫苗板块股价集体大涨,已有基金低谷期入场“抄底”
整体而言,国内疫苗行业仍在经历低谷,且行业高度分散。截至目前,已有50家中国疫苗企业获得注册批件,其中30家仅有1-2款产品。
医保个账支付自费苗或“松绑”,哪些疫苗有望惠及?
一些地方陆续允许职工医保个账或家庭共济支付部分非免规疫苗,进而形成了“国家边界+地方探索"的差异化格局。
