分享到:
- 微信
- 微博
AI帮你提炼, 10秒看完要点
智能挖掘相关板块, 定位投资机会


AI速读
节省{{readTime}}分钟阅读时间 {{aisd}}
AI生成 免责声明
上海市药品监督管理局印发《上海市第二类医疗器械优先审批程序》。
上海市药品监督管理局印发《上海市第二类医疗器械优先审批程序》。
其中提出,对符合下列条件之一的本市第二类医疗器械注册申请实施优先审批:(一)列入国家科技重大专项、重点研发计划或者本市科技重大专项、科技创新行动计划的;(二)诊断和治疗罕见病,且具有明显临床优势的;(三)诊断和治疗老年人特有和多发疾病,且目前尚无有效诊断或治疗手段的;(四)专用于儿童,且具有明显临床优势的;(五)境内无同品种产品获准注册且具有明显临床优势的,或者境内同品种获批注册较少且无法满足临床需求的。
举报
第一财经广告合作,请点击这里
此内容为第一财经原创,著作权归第一财经所有。未经第一财经书面授权,不得以任何方式加以使用,包括转载、摘编、复制或建立镜像。第一财经保留追究侵权者法律责任的权利。如需获得授权请联系第一财经版权部:banquan@yicai.com
相关阅读

专访前GE医疗中国总裁兼CEO张轶昊:外企本土化,要有“创始人心态”
张轶昊认为,本土化的成败取决于是否构建无法被替代的全链条核心竞争力,并将信任赋予中国团队。

波士顿科学临港基地获首证,打破高值医械耗材“临期焦虑”
波士顿科学公司临港工厂首期已建成国内首条血管内超声导管自动化生产线,通过持续加码中国的本土化战略,加速高端医疗设备在中国市场的可及性。

直击中东变局|中东紧张局势升级,对中国医疗企业出海影响几何?
中国企业出海中东的门槛其实并不低。

物流中断、提货暂停:中东冲突按下中国医械出海“暂停键”,长期布局仍坚定
近年来,在中国医疗器械企业出海版图中,中东就成为热门地之一。出海中东的国产医疗器械企业:国际物流承压,有企业暂停人员外派。
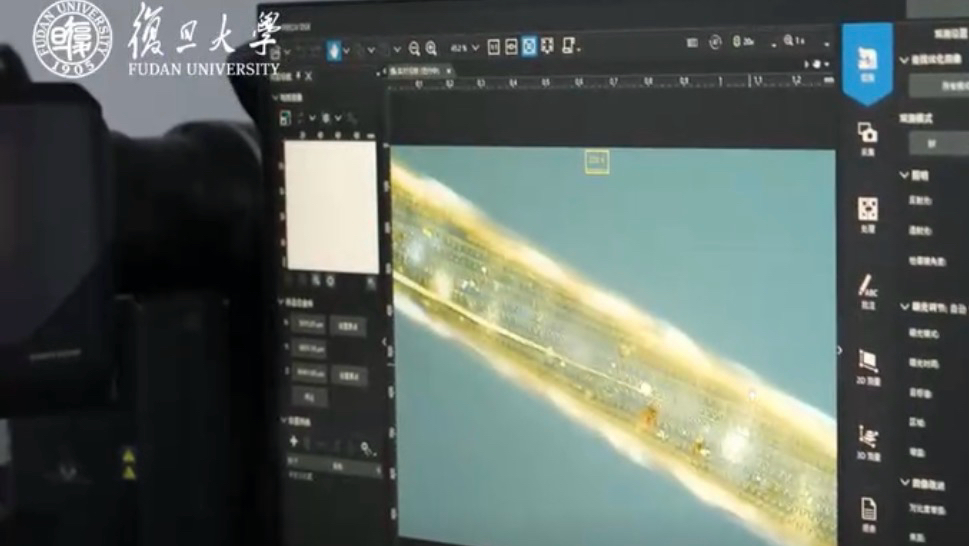
中国研制纤维芯片成果再登顶刊!“头发丝里实现大规模集成电路”
中国团队在国际上率先研制出“纤维芯片”。要实现纤维器件的更大规模化应用,必须攻克“芯片”的核心技术壁垒,包括空间限制、光刻适配以及稳定性挑战。
一财最热