分享到:
- 微信
- 微博


{{aisd}}
AI生成 免责声明
12月9日,国内首个PD-L1药物英飞凡(俗称“I”药)获得批准,本该祝贺,却让我想起了一个悲伤的故事。
朋友的母亲在2017年患晚期肺癌,国内医生告诉他没有治疗方法,生存期只有数月。在绝望中,朋友了解到了PD-1药物O药(英文名Opdivo,中文名欧狄沃)。O药2014年获得美国药品监督管理局批准,但当时在国内还没有被批准使用。
朋友费劲周折,找遍药托,从香港买到正品药物。没料到的是,因为药物在国内没有获批且有可能有非常强的用药反应,找到敢于用药的医院和医生并不容易。朋友花了三个星期的时间找医院和医生,等所有安排妥当的时候,老人的病情已经恶化到不适合再用药了。几个月后,老人去世了。
恰恰在此后不久的2018年6月,O药在国内就被批准了。一个创新药物晚批准一个月,失去的是成千上万个本可以延长数年的生命。
难题
朋友碰到的问题,涉及复杂的药品研发、上市、审批和使用。
药品上市。此处的上市不是股票上市,而是药物获得药品监管机构的许可,能够上市销售用于临床。在上市之前,药品需要经过一期临床实验、二期临床实验、三期临床实验,通过大规模的人体实验,验证药物的安全性和有效性。一个美国公司的药物获得美国药品监管机构的审批,想要在中国上市,还要获得中国药品监管机构的审批。
“局部”绝症。从全球范围来看,美国是创新药研发的大本营,中国正在迎头赶上。有的药物在国内没有批准上市,在中国生存期只有数月的病,可能在有药可用的美国,生存期就是数年。所以,碰到绝症,要看是不是在其他国家有创新的治疗方法。当然,如果在医疗水平落后的地区,三四五线城市,也存在被局部宣判治不了,但到了北上广的大医院,其实根本不是事儿的情况。
试验药品。如果没有已经获批上市的新药,还有最后一个“碰运气”的方法,那就是参加创新药物的临床试验。既然是试验,就有试验失败的风险。从全球范围看,药物从进入临床试验到能上市批准的概率只有10%。碰运气的策略是最好参加较后期的临床试验,虽然三期临床并不一定代表成功的概率更大,但是至少说明安全性在一期和二期临床中获得了较好的效果。
费用问题。创新药物一般较贵。例如,O药在国内获批后的价格是100mg/10ml,9260元,一个月的治疗费用约3.6万元,比港澳购药的5万多元已经便宜很多了。参加临床试验,一般不需要支付费用,都是药厂支付所有的费用。所以,药物的研发成本很高。
但也有个别例外,近日,美国基因治疗公司Libella宣布,世界首个逆转衰老的收费临床试验获得批准。这个试验使用一种病毒作载体,将端粒酶逆转录酶递送到人体中,延长端粒长度从而实现逆转衰老,有望让人类逆转衰老20年。要用病毒做载体,听起来有点可怕,但是如果试验成功了,真能多活20年啊,所以,参与试验的人要付费100万美元,换取多活20年的可能性。
生命真的无价,不同的人有不同的定价。
商战
PD1/PD-L1是一种免疫疗法。科学家发现,癌症的发展是因为癌细胞非常狡诈地躲过了免疫细胞T细胞的追杀。
PD全称为Programmed Death,中文翻译为“程序性死亡”。PD-1是位于T细胞表面的一种免疫抑制分子,当PD-1接通“程序性死亡”的信号时,会减少T细胞激活,甚至让T细胞“程序性死亡”,从而使T细胞降低对癌细胞的识别,癌细胞达到了“迷惑”T细胞的目的。“接通”的时候,需要一种配体和PD-1结合,这就好比有插座就必须要有插头才能通电一样。这个配体便是PD-L1。
如果能抑制PD-1和PD-L1,就能让T细胞免受迷糊,继续杀死癌细胞。上文所说的O药和I药就是PD-1/PD-L1抑制剂。
但是,科学研究从实验室到商业化的难度并不比科学研究本身简单。全球首个PD-1药物叫K药,它数次差点胎死腹中,诞生的历程可谓一波三折、惊心动魄。
K药最初由一家荷兰公司研发。2003年的时候,这家叫欧加农的制药公司,希望能活化PD-1受体,从而治疗免疫性疾病。他们的想法是“活化”,而非“抑制”,与现在的方向正好相反,且研发的适应症也不是癌症。
有意思的是,到2005年,他们没有找到活化PD-1的抗体,却意外发现了抑制PD-1的抗体。但他们不知道怎么使用这些抑制剂,为了不浪费之前的研究,他们决定在充满争议的癌症免疫疗法上进行尝试。
2年后,欧加农找到了现在K药使用的抗体,公司研发人员非常兴奋。但是还没等进一步推进,公司就被先灵葆雅公司并购了。先灵葆雅当时是美国第七大药企。新东家的管理层认为调节T细胞治疗癌症的风险太大,难以控制细胞因子风暴,这个项目被移出了重点项目清单,变成了可做可不做的项目。没过多久,先灵葆雅又被别人收购了。这次的东家是默沙东。
默沙东是一家有400亿美元销售额、100多年历史的医药巨无霸。比前面的一次收购更惨,默沙东进来后,把PD-1抗体团队解散了,准备把PD-1的研发成果卖掉。
为什么呢?虽然默沙东一年研发费用有100亿美元,不差钱,但肿瘤药物不是默沙东的传统优势和主攻方向。这就是在生物医药领域,很多小公司更有可能做出创新的原因。在大公司中,虽然研究经费很多,但是研发管线也很多,需要服从公司战略,研究经费向重点项目倾斜。创业公司则不同,全部资金主攻一个药物,在单一品种上投入的资金,可能比大公司还多。
转机发生在竞争对手的疏忽上。2010年,另一家大型药企施贵宝制药在《新英格兰医学杂志》上首次发表了伊匹单抗(Ipilimumab,商品名Yervoy)安全有效的临床研究结果。伊匹单抗是另一个免疫检验点CTLA-4的抑制剂,与PD-1抗体有些类似。
这一结果预示了“免疫检验点抑制剂”的可行性,改变了当时肿瘤免疫治疗领域的主流观点。同时,有消息称,施贵宝制药的另一个检验点抑制剂PD-1抗体在临床一期也已初见成效。竞争对手泄露了天机。
默沙东虽然大,但是商业反应还是很迅速的,他们敏锐地看到了这一重大进展,发现自己手上竟然有现成的PD-1抗体。于是,默沙东把准备卖掉的PD-1又拿了回来,迅速重新组建研发团队。
冥冥之中自有天意,比施贵宝落后的默沙东,碰上了好政策。2012年,美国食品药品监督管理局(FDA)计划实施了一种称为“突破性疗法认定”(Breakthrough designation,简称BTD)的政策,旨在使新药的批准更加合理和快速。默沙东在第一时间就获得了这个非常重要的信息,在这项新政策被广为宣传之前,率先申请并于2013年1月获得了BTD资格,成为BTD政策推出以来,第二个获此政策认可的实验药物。
历经波折,占尽了天时地利人和的默沙东的K药终于成功实现了弯道超车,于2014年9月4日被批准上市,成为全球第一个被批准用于晚期黑色素瘤治疗的PD-1抗体原研新药,比施贵宝的O药早上市3个月,载入史册。
药神
此后的发展非常顺利。
默沙东的K药在2018年的全球销售额逼近500亿元人民币(71亿美元),当时默沙东收购先灵葆雅的时候,花了410亿美元,不小心捡到了PD-1这个宝贝。2013年到现在,公司股价翻倍,市值涨了1000多亿美元。
美国科学家詹姆斯·艾利森(James P. Allison)和日本医学家本庶佑(Tasuku Honjo),因为在PD-1/PD-L1研究中的贡献获得了2018年的诺贝尔奖。
到目前为止,全球的PD-1/PD-L1药物一共有9款。值得庆祝的是,这9款中,有三款是我国国产的PD-1药物,他们的生产厂商分别是君实生物、恒瑞医药和信达生物。君实生物是第一款获批的国产PD-1,于2018年12月获批,比美国晚了6年。尽管如此,这是非常值得自豪的成绩,表明我国的生物制药产业已经逐步迈入了世界最先进的行列。
君实生物原本是一家新三板公司,2018年在香港生物科技医药板块上市,目前在申请科创板上市。君实生物的PD-1在获批后的半年时间里已经取得了3亿元的销售额,公司预计该产品的销售峰值可能超过150亿元。
中国资本市场的好公司并不少,需要有发现珍珠的眼光。
2017年10月,中办、国办印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,基本解决了药品注册申请积压问题,一批临床急需新药优先获准上市。2018年,中国批准了54种创新药物,远多于2016年的6种新药。在去年批准的药品中,许多是在“优先审查”制度下生产的急需药品。
5年前,中国每年因为癌症死亡的人数高达200万,现在的数据可能更多。一个创新药物提前上市1个月,哪怕能让5万人,延长2年的生命,那就是10万年的生命。药神的含义正如此。
真正的药神是以上这些科学家、医生、创新药企、创新的监管机构,以及支持药企研发的风险投资机构和资本市场。
[作者系领复资本创始人,注册金融分析师(CFA),风险投资人,专注医疗高科技投资]
第一财经获授权转载自“秦朔朋友圈”微信公众号,原标题:《10万年与500亿:又一款抗癌神药获批的背后》
文章作者
默沙东被低估的“王牌”?“坏胆固醇”克星催生百亿美元规模市场
LDL-C过高导致全球慢病死亡风险激增6.4倍,堪称“最隐匿的生命威胁”。

默沙东宣布67亿美元收购生物技术公司Terns Pharma
默沙东正在应对重磅肿瘤药物Keytruda的专利到期。
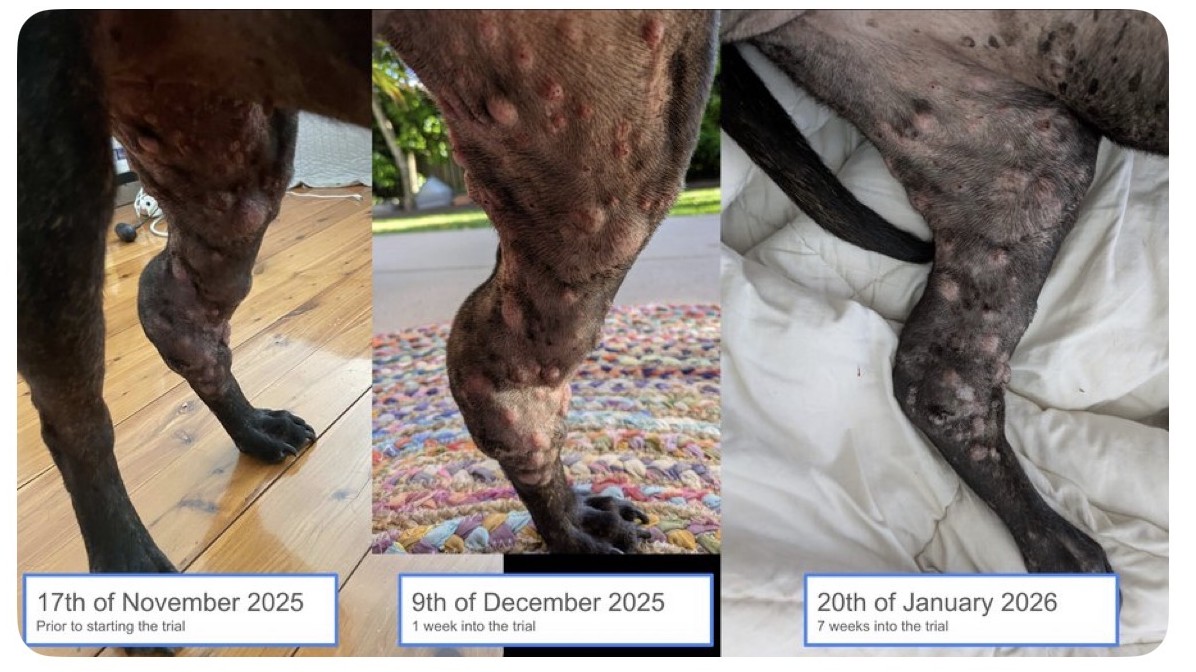
程序员用AI手搓疫苗抢救患癌爱犬,马斯克等大佬点赞
动物实验转化为人类临床仍有漫长道路。
政府工作报告连续三年点名“创新药”,今年聚焦商保支付保障
加快发展商业健康保险,推动创新药和医疗器械高质量发展

《药品管理法实施条例》超9成条款更新,创新药企受益明显
《条例》鼓励新药研制与创新,加强市场独占期、数据保护、分段生产等是企业、行业关注的核心。
