分享到:
- 微信
- 微博
国家食品药品监督管理局6月25日发布通报,提示关注脉络宁注射液的严重不良反应,对此,金陵药业公告称,公司认为本期通报不会对脉络宁注射液的销售带来较大影响。
国家食品药品监督管理局6月25日发布通报,提示关注脉络宁注射液的严重不良反应,对此,金陵药业(000919.SZ)6月26日晚间公告称,公司认为本期通报不会对脉络宁注射液的销售带来较大影响。
据公告,2011年度公司脉络宁注射液销售收入为53590.20万元,占销售总收入的23.74%。
根据药监局此前通报内容,其提示喜炎平注射液和脉络宁注射液易发生过敏反应,并建议医护人员应严格按照说明书规定的用法用量给药、谨慎联合用药,还要求药品生产企业加强临床合理用药的宣传、完善生产工艺、提高产品质量标准。
通报显示,2011年度,药监局收到有关脉络宁注射液药品不良反应/事件病例报告1500例,其中严重病例报告189例。
公司称,2011年度脉络宁注射液的总销售量为8500万支,按疗程人均最大用量估算,全年使用例数约为303.5714万例,上述报告的不良反应发生率为0.494‰,为罕见范畴,严重不良反应发生率为0.062‰,为十分罕见范畴。
公司并称,多年来始终关注着药品不良反应问题,为了保证产品安全、有效和质量可控,做了多方面工作避免脉络宁注射液不良反应的发生。
鉴于公司对脉络宁注射液不良反应问题所做的大量工作,公司认为本期通报不会对脉络宁注射液的销售带来较大影响。
不过金陵药业26日开盘之后即跌停,全天以8.40元的跌停价报收。
举报
相关阅读

上海市药监局印发《上海市第二类医疗器械优先审批程序》
上海市药品监督管理局印发《上海市第二类医疗器械优先审批程序》。

全力支持高端医疗器械重大创新,国家药监局发布十大举措
对符合要求的国内首创、国际领先,且具有显著临床应用价值的高端医疗器械继续实施创新特别审查。
国家药监局:加强人工智能、生物材料“揭榜挂帅”产品的注册指导
加强人工智能、生物材料“揭榜挂帅”产品的注册指导,配合相关部门出台基于脑机接口技术的医疗器械产品支持政策。
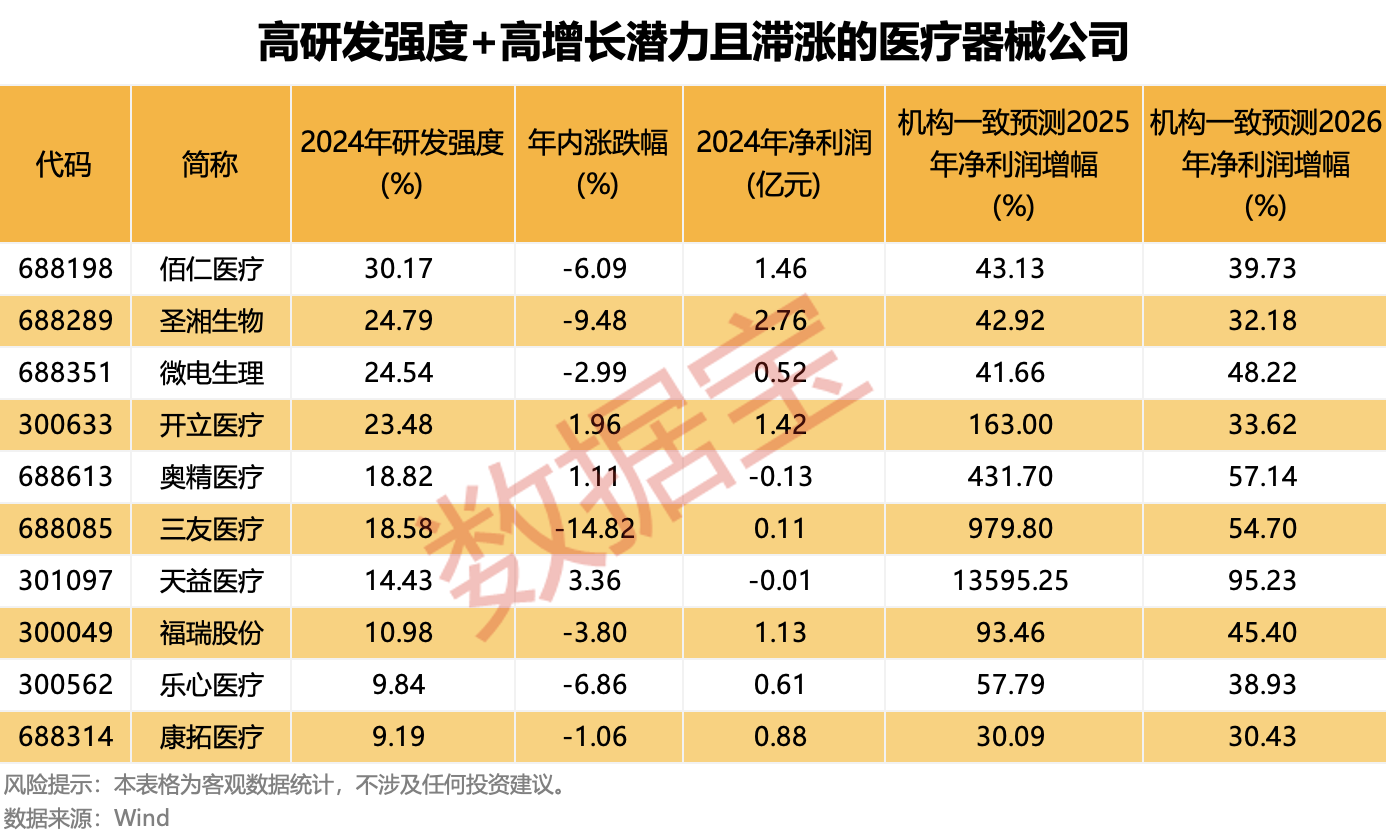
国家药监局重磅举措,10只滞涨股具备“高研发强度+高增长潜力”双重特征
国家药监局重磅举措,10只滞涨股具备“高研发强度+高增长潜力”双重特征

替尔泊肽注射液多剂量预装笔中国上市
替尔泊肽注射液多剂量预装笔中国上市
一财最热