分享到:
- 微信
- 微博


{{aisd}}
AI生成 免责声明
今年年初,国家药监局(NMPA)批准了卫材公司的阿尔茨海默病(AD)一类新药仑卡奈单抗注射液(中文商品名:乐意保)的上市申请,适应证为治疗早期阿尔茨海默病。
这款药物在中国的最新上市进展如何?2月5日,第一财经记者从卫材中国公司方面了解到,这款药物预计今年下半年在中国上市,但上市初期能够获得治疗的首批中国患者数量将相对有限,这主要受到诊断不足等因素影响。
能否纳入医保
卫材日本总部发言人称,到明年年初,中国预计将有1500名患者能够首批用上这种治疗药物。而随着阿尔茨海默病诊断方法的突破改进,预计到2025年,该药物增长将显著加速。
对于1500名首批患者的预估数据,卫材中国方面对第一财经记者表示,目前官方并没有确切的预估数据,受到很多因素影响。
据卫材公司目前的公开信息,乐意保上市后预计定价2508元,即一个60公斤体重的患者月均治疗费用约1.5万元,年治疗费用约18万。这款药物预计将在2024年7月份在国内上市。卫材也在评估将这款药物纳入医保的可能性。
卫材方面称,中国是世界上老龄化速度最快的国家之一,也是卫材在阿尔茨海默病领域最重要的市场之一,乐意保在中国的潜在增长是巨大的。
在一项公开发表的临床试验中,这种每月输注两次的阿尔茨海默病治疗药物能使早期患者的病情进展速度减缓27%。
卫材预计,中国预估有1700万早期阿尔茨海默病患者,随着阿尔茨海默血液检测等新的诊断方法在中国的逐步推进,有望在未来大幅推动阿尔茨海默疗法适用患者的比例。
“阿尔茨海默病控制关键在于早期的预防、诊断和治疗,但是目前来看,早期就诊求医的比例仍然非常低,对阿尔茨海默病的诊断需求很大。”复旦大学附属华山医院神经内科郁金泰教授对第一财经记者表示。
目前乐意保治疗的患者需要接受认知测试、核磁共振检查,基因测试或者淀粉样蛋白水平的相关检查,以综合评估是否接受治疗,以及用药管理的方案。
早期诊断不足
在国内,早期就诊率低是阿尔茨海默病防治的一个重要挑战。根据华福证券研究所发布的研究报告,2019年,我国有71.4%的阿尔茨海默病患者从未因痴呆症就诊过,97.2%轻度认知障碍患者没有接受诊疗。接受就诊的患者中,约80%为中重度患者。
根据《中国阿尔茨海默病痴呆诊疗指南》,目前针对阿尔茨海默的检查主要有临床评估、脑影像学检查和实验室检查三种方式,临床评估作为常规检查,性能一般,目前阿尔茨海默症检测金标准是PET/CT脑显像或脑脊液检测,但脑脊液检测需要穿刺,因此侵入性低的PET/CT脑显像是目前主要的诊断方式。寻找方便、无创、可靠的外周血阿尔茨海默病标志物将有助于突破这一瓶颈。
第一财经记者发现,目前卫材与京东健康合作开通了“银发通”的App和小程序,该平台是目前获取这款药物的公开通道。患者在进行线上脑健康自测,并与神经领域专家进行线上咨询,获得专业指导;搜寻附近医院的记忆门诊或神经内科进一步线下就医确诊;最后,通过“银发通”平台线上预约药物,以在药物上市后获得治疗机会。
阿尔茨海默病治疗药物的研发难度极大,卫材这款最新在中国获批的药物为仑卡奈单抗,这是一种人源化抗可溶性β淀粉样蛋白(Aβ)单克隆抗体,也是首款通过去除致病物质来抑制阿尔茨海默病发展的新型药物。
与此同时,礼来公司也在开发一种名为多纳奈单抗(donanemab)的类似治疗方法。根据礼来去年5月公布的一项临床研究结果,多纳奈单抗在18个月内将某些早期阿尔茨海默病患者的认知和功能下降速度减缓了35%,优于仑卡奈单抗的27%。此外,相较于仑卡奈单抗每两周给药一次的频率,多纳奈单抗为每四周用药一次,降低了用药频率。
礼来公司也正在寻求中国对该药物的批准。去年10月,礼来向中国NMPA提交新药上市申请并获得受理。去年7月,礼来已经向美国FDA递交审批申请。
如需获得授权请联系第一财经版权部:banquan@yicai.com
文章作者
欧洲两项大规模研究颠覆认知,心血管医生的“第三只眼”失灵了?
与单纯冠脉血管造影指导相比,使用IVUS引导的PCI手术,并未显著降低患者的主要不良临床事件风险。
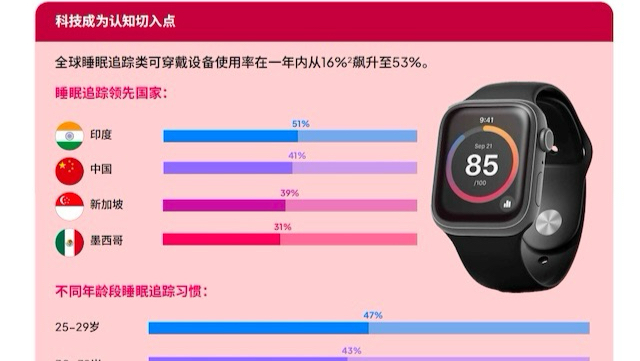
使用可穿戴设备追踪睡眠的人更多了,但缘何这种疾病的诊断率却仅有1%
睡眠科技的兴起令人鼓舞,但仅靠监测还不够。
85岁以上4人中就有一个罹患阿尔茨海默病?血检大规模推广仍存争议
随着研究人员开发出更多基于血液的生物标志物,该领域将能够更好地利用这些工具,并提供更多关于大脑健康状况的信息。

中国科研团队研发出AI看病系统 诊断罕见病“有根有据”
这套名为DeepRare的系统,被称作全球首个“推理过程可追溯”的罕见病智能医生。
多款试剂已投入临床应用,“滴血测痴呆”时代来临
在临床上大规模地采用血液检测的方法,将有助于阿尔茨海默病的早诊早筛,且可使患者尽早获得治疗。目前已经上市的新型AD药物,都仅对早期阿尔茨海默病患者产生疗效。
